Case study: Supercomputer maakt communicatie tussen hersencellen zichtbaar
Het brein is erg belangrijk voor mensen, maar we weten nog niet precies hoe het werkt. Bijvoorbeeld: Wat is geheugen? Hoe denken we? Om dichterbij het antwoord op dit soort vragen te komen, onderzoeken scheikundigen Bert Janssen en Dimphna Meijer van de Universiteit Utrecht de eiwitten die communicatie tussen hersencellen mogelijk maken.
Gesprek tussen hersencellen
Communicatie tussen de cellen in onze hersenen is essentieel voor het functioneren van ons brein en de ontwikkeling ervan. Dit ‘gesprek’ wordt meestal mogelijk gemaakt door proteïnen (eiwitten). De onderzoeksgroep Crystal and Structural Chemistry van dr. Bert Jansen aan de Universiteit Utrecht onderzoekt hoe deze eiwitsystemen signalen initiëren en omzetten tussen de cellen in onze hersenen
’Begrijpen hoe hersenen werken’
“We willen een fundamenteel begrip krijgen van hoe de hersenen werken op moleculair niveau”, vertelt Dimphna Meijer, postdoc in de groep van Janssen. “We bestuderen dus niet wat er misgaat bij een ziekte, maar waarom het goed gaat in gezonde hersenen. Dan kan je uiteindelijk ook beter begrijpen wat er gebeurt als het misgaat.”
Eiwit Teneurin: 1000 keer kleiner dan een haar
Het punt waarop de interactie tussen twee neuronen (zenuwcellen) plaatsvindt, heet synaps. Janssen en Meijer hebben met Teneurin een specifiek eiwit in kaart gebracht dat ervoor zorgt dat die synapsen aan elkaar blijven zitten. “Zo’n eiwit is 20 nanometer lang”, zegt Janssen. “Dat is 1000 maal kleiner dan de doorsnede van een haar. Met een gewone microscoop kun je hem niet eens zien; daarvoor gebruiken we een elektronenmicroscoop.”
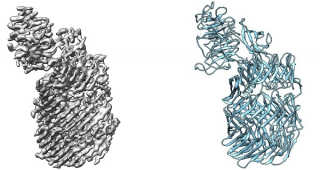
Het Teneurin-eiwit
Nieuwe en revolutionaire technologie
Cryo-elektronenmicroscopie is een relatief nieuwe en revolutionaire technologie (aldus Nature), die in 2017 is beloond met een Nobelprijs. Deze techniek vuurt bundels elektronen af op diepgevroren eiwit-specimens om de structuur van de biomoleculen te bekijken. De hieruit verkregen beelden worden in de computer omgezet in 3D-beelden, door opnames te combineren die vanuit verschillende hoeken zijn gemaakt. Hierbij wordt onder meer de software Relion ingezet, ontwikkeld door de Nederlander Sjors Scheres, die promoveerde aan de Universiteit Utrecht en nu een onderzoeksgroep leidt in Cambridge.
Hulp van supercomputer: 2,1 miljoen core-uren
Voor dat omzetten heb je veel computerkracht nodig, en de scheikundigen zetten daarvoor een GPU-cluster in van de Nationale Supercomputer. De supercomputer gebruikt vele cores (processorkernen) tegelijkertijd; op een gewone laptop met 4 cores zouden deze berekeningen bijna 60 jaar kosten. De onderzoeksgroep heeft flink wat capaciteit toegewezen gekregen: 2,1 miljoen core-uren, waarvan in een jaar tijd al een derde is gebruikt. GPU’s (graphics processing units) kunnen de benodigde rekentaak veel sneller uitvoeren dan de traditionele CPU’s (core processing units). Meijer: “SURF heeft ons geholpen om optimaal gebruik te maken van onze algoritmes op het GPU-cluster.”
11 terabyte aan data
“Om een driedimensionale afbeelding van het eiwit in een hoge resolutie te krijgen, hebben we een miljoen opnames nodig, die we vervolgens met elkaar combineren. Onze dataset begon met 11 terabyte aan data. Die moesten allemaal naar SURF gekopieerd worden, dat duurde wel 3 dagen. Tijdens het verwerken - en dat duurt maar een paar uur - wordt de hoeveelheid data nog eens verdubbeld. Het uiteindelijke 3D-beeld wordt dan weer gereduceerd tot iets wat op een usb-stickje past: 200 MB.”
Nieuwe vragen over Teneurin-eiwit
Het 3D-beeld van het Teneurin-eiwit heeft geresulteerd in een eerste publicatie binnen dit project. Nu ze hem in beeld hebben, kunnen de onderzoekers het eiwit verder bestuderen. Janssen: “De belangrijkste conclusie is dat Teneurin er heel anders uitziet dan alle traditionele ‘cell adhesion molecules’, proteïnen die betrokken zijn bij het aan elkaar verbinden van cellen. Het gekke is dat het qua structuur heel erg lijkt op een bacterieel eiwit. Nu we gedetailleerd weten hoe het is opgebouwd, hoe de functionele units eruit zien en waar ze zitten ten opzichte van elkaar, kunnen we verder. Nu willen we begrijpen hoe het eiwit werkt. We weten ook nog niet waarom hij er zo anders uitziet. En zoals gebruikelijk komen er uit deze ontdekking ook weer veel nieuwe vragen voort.”
Publicatie
In deze video vertelt Bert Jansen over zijn onderzoek.

